Bedruckte Bäckertüten oder gefärbte Servietten: Gesundheitliche Beeinträchtigungen sind durch die Freisetzung bestimmter Farbmittelbestandteile nicht zu erwarten Neue Daten erlauben aktualisierte Bewertung von Naphthol AS, NAAX, NDPA und HNS in Lebensmittelkontaktmaterialien
Ersetzt die Stellungnahme Nr. 037/2019 vom 26. September 2019
Darum geht es:
Materialien, die bestimmungsgemäß oder erwartbar mit Lebensmitteln in Berührung kommen, heißen auch Lebensmittelkontaktmaterialien oder Lebensmittelbedarfsgegenstände. Zu Lebensmittelkontaktmaterialien aus Papier und Pappe zählen neben Kartonverpackungen, Bäckertüten und Servietten auch andere Utensilien wie Muffinformen und Trinkhalme. Bei ihrer Produktion werden zahlreiche Hilfs- und Veredelungsstoffe eingesetzt. Ein Beispiel sind Farbmittel, mit denen manche dieser Produkte eingefärbt oder (bunt) bedruckt werden.
In der vorliegenden Risikobewertung hat das Bundesinstitut für Risikobewertung (BfRkurz fürBundesinstitut für Risikobewertung) auf Basis neuer Daten zur Stabilität und Toxizität geprüft, ob mit der Aufnahme bestimmter Stoffe in Farbmitteln (Naphthol AS, HNS, NAAX und NDPA) gesundheitliche Risiken für Verbraucherinnen und Verbraucher einhergehen. Dies ist der Bewertung zufolge für die nachgewiesenen Mengen dieser Stoffe nicht zu erwarten.
Naphthol AS, NAAX, NDPA und HNS sind sehr wahrscheinlich Ausgangsstoffe, Verunreinigungen oder Abbauprodukte bestimmter Farbmittel, sogenannter Azofarbstoffe und -pigmente. Um zu bestimmen, welche Mengen dieser Stoffe aus Lebensmittelkontaktmaterialien ggf. in Lebensmittel übergehen, nutzten die Forschenden die Kaltwasserextrakt-Methode. Die Proben wurden dabei 24 Stunden lang bei Raumtemperatur mit dem Wasser – stellvertretend für Lebensmittel – in Kontakt gebracht. Anschließend wurden die Gehalte der vier Stoffe im Wasser bestimmt.
Für keine der vier Verbindungen gibt es gesetzlich festgelegte Migrationsgrenzwerte oder abgeleitete gesundheitliche Richtwerte. Das BfRkurz fürBundesinstitut für Risikobewertung hat deshalb ausgehend von toxikologischen Daten zu den genannten Verbindungen sowie von Stoffen mit ähnlicher chemischer Struktur und durch computergestützte Vorhersagemodelle gesundheitlich akzeptable Aufnahmewerte abgeleitet.
Für HNS sind demnach bei einem 60 kgkurz fürKilogramm schweren Menschen bei einer lebenslangen Aufnahme von 360 µgkurz fürMikrogramm (Mikrogramm) pro Tag keine gesundheitlichen Beeinträchtigungen zu erwarten. Die aus den untersuchten Proben übergehenden Mengen an HNS übersteigen diesen Wert nicht und stellen somit kein erhöhtes Gesundheitsrisiko dar.
Für die Substanzen Napthol AS, NAAX und NDPA war die Datenlage bisher für eine gesundheitliche Bewertung nicht ausreichend. Wie in einer Externer Link:früheren Version dieser Stellungnahme dargestellt (Nr. 37/2019), gab es zudem Hinweise, dass diese Stoffe bzw. ihre möglichen Stoffwechselprodukte im menschlichen Organismus erbgutverändernde und krebserzeugende Eigenschaften besitzen könnten. Die mittlerweile vorliegenden neuen Daten zu möglichen Stoffwechselprodukten zeigten, dass ein Abbau der Stoffe zu erbgutverändernden Stoffwechselprodukten – wenn überhaupt – nur in sehr geringem Maße stattfindet. Die vorher nicht vorhandenen und jetzt ebenfalls neu vorliegenden Tests zu NDPA zeigten keine erbgutverändernden Effekte. Aus einer Migration von Naphthol AS, NAAX bzw. NDPA von bis zu 50 Mikrogramm (µgkurz fürMikrogramm) pro Kilogramm (kgkurz fürKilogramm) Lebensmittel ergeben sich entsprechend nach aktueller Datenlage keine Gesundheitsrisiken für Verbraucherinnen und Verbraucher. Lediglich für einzelne Proben (2 von insgesamt 51 untersuchten Proben) wurde eine Migration oberhalb von 50 µgkurz fürMikrogramm/kgkurz fürKilogramm Lebensmittel für Naphtol AS beobachtet. Die toxikologische Datenlage ist aktuell nicht ausreichend, um diese Migration gesundheitlich bewerten zu können. Das BfRkurz fürBundesinstitut für Risikobewertung empfiehlt entsprechend, dass kein Übergang von Naphtol AS (sowie von NAAX und NDPA) oberhalb von 50 µgkurz fürMikrogramm/kgkurz fürKilogramm Lebensmittel stattfinden sollte.
Verpackungspapier für Backwaren enthielt häufig mehrere der untersuchten Substanzen und gab diese in den Wasserextrakt ab. Andere Probengruppen wie Trinkhalme, Muffinformen und Servietten zeigten insgesamt deutlich weniger und deutlich geringere Freisetzungen. In jeder Probengruppe gab es zudem auch Proben, in denen gar keine Freisetzung von Naphthol AS, NAAX und NDPA nachgewiesen werden konnte. Das BfRkurz fürBundesinstitut für Risikobewertung empfiehlt Herstellern, ihre Rohstoffe und Endprodukte auf Verunreinigungen mit diesen Substanzen bzw. deren Freisetzung zu prüfen und ggf. Alternativen zu den verwendeten Materialien zu suchen.
1 Gegenstand der Bewertung
Im Folgenden bewertet das BfRkurz fürBundesinstitut für Risikobewertung die vorliegenden Daten der Lebensmittelüberwachung aus dem Jahr 2018 zur Freisetzung der Verbindungen Naphthol AS (CAS 92-77-3, auch 3-Hydroxy-2-naphthanilid), N-Acetoacetyl-m-xylidin (CAS 97-36-9, NAAX), N-(2,4-dimethylphenyl)-acetamid (CAS 2050-43-3, NDPA) und 3-Hydroxy-2-naphtoesäure (CAS 92-70-6, HNS) aus verschiedenen Lebensmittelkontaktmaterialien (Food Contact Materials; FCM) aus Papier und Karton im Kaltwasserextrakt. Bei der Überwachungsbehörde eines Bundeslandes wurden die Kaltwasserextrakte verschiedener FCM aus Papier und Karton wie Servietten, Kartonverpackungen und Trinkhalme auf Rückstände von Farbstoffen, deren Abbauprodukten und herstellungsbedingten Verunreinigungen hin untersucht. Der Kaltwasserextrakt wurde dabei entsprechend DIN EN 645 und die Analyse mittels LC-MS/MS durchgeführt. Dabei wurden in einigen Proben die genannten vier Verbindungen (Abbildung 1) quantitativ bestimmt.
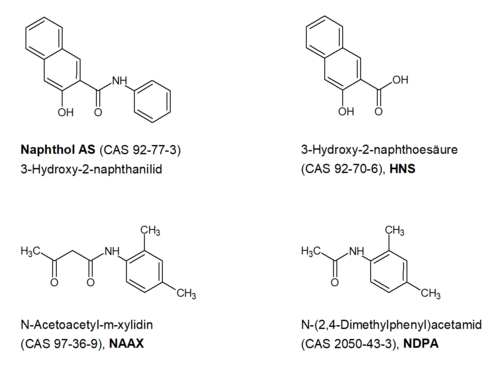
Das BfRkurz fürBundesinstitut für Risikobewertung hatte bereits 2019 eine gesundheitliche Bewertung der in den Migrationsexperimenten bestimmten Mengen dieser Stoffe durchgeführt. Aufgrund neu vorgelegter Daten zur Stabilität und Toxizität einiger der Verbindungen, hat das BfRkurz fürBundesinstitut für Risikobewertung die Freisetzungsmengen neu bewertet.
2 Ergebnis
Es existieren keine gesetzlichen oder normativen Grenzwerte für die Freisetzung der in Abbildung 1 gezeigten Verbindungen aus Papier und Karton. Das BfRkurz fürBundesinstitut für Risikobewertung hat, ausgehend von toxikologischen Daten zu den genannten Verbindungen und chemisch/strukturell ähnlichen Verbindungen sowie in silico-Daten, gesundheitlich akzeptable Aufnahmewerte abgeleitet.
Danach sind bei einer Aufnahme von 360 µgkurz fürMikrogramm HNS bei einem 60 kgkurz fürKilogramm schweren Menschen pro Tag keine gesundheitlichen Beeinträchtigungen zu erwarten.
Für Naphthol AS, NAAX und NDPA hat das BfRkurz fürBundesinstitut für Risikobewertung aus den vorhandenen Daten abgeleitet, dass eine Freisetzung vermutlich genotoxischer bzw. kanzerogener Anilinderivate, wenn überhaupt, nur in Mengen stattfindet, bei denen kein genereller Anlass zu einer erhöhten gesundheitlichen Besorgnis besteht: Da umfassende toxikologische Langzeitstudien in vivo zu Naphthol AS, NAAX und NDPA fehlen, erfolgte die Bewertung auf der Grundlage einer in vitro Studie sowie des „Threshold of Toxicological Concern“ (TTCkurz fürThreshold of Toxicological Concern)-Konzeptes. Nach dem TTCkurz fürThreshold of Toxicological Concern-Konzept ist die tägliche Aufnahme eines genotoxisch kanzerogenen Stoffes von höchstens 0,15 µgkurz fürMikrogramm pro Person nicht mit einem erhöhten Grund zur Besorgnis verbunden. Für nicht-genotoxische Substanzen ist im Bereich FCM nach dem „Note for Guidance“ der Europäischen Behörde für Lebensmittelsicherheit (EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit)) eine tägliche Aufnahmemenge von bis zu 50 µgkurz fürMikrogramm pro Person gesundheitlich akzeptabel (EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit) Panel on Food Additives et al.kurz füret alii (lat. "und andere") 2008). Mit der typischerweise zugrunde gelegten Annahme (Verzehr von einem Kilogramm Lebensmittel, das im Kontakt mit dem FCM war, pro Tag) ergibt sich daraus eine tolerierbare Migration von bis zu 50 µgkurz fürMikrogramm pro kgkurz fürKilogramm Lebensmittel.
HNS, NAAX und NDPA waren in nahezu der Hälfte der untersuchten 51 Proben nachweisbar, Naphthol AS in 10 Proben. Auffällig war vor allem Verpackungspapier für Backwaren, das häufig mehrere der Substanzen enthielt und in den Wasserextrakt abgab. Andere Probengruppen wie Trinkhalme, Muffinformen und Servietten zeigten insgesamt deutlich weniger und deutlich geringere Freisetzungen. In jeder Probengruppe gab es Proben, in denen Naphthol AS, NAAX und NDPA nicht nachgewiesen wurden. Die gemessenen Migrationswerte für HNS bzw. NAAX und NDPA waren alle kleiner als 360 µgkurz fürMikrogramm/l bzw. kleiner als 50 µgkurz fürMikrogramm/l. Entsprechend ergibt sich aus diesen Migrationswerten kein erhöhtes Gesundheitsrisiko. Für einzelne Proben (n = 2) wurde eine Migration oberhalb von 50 µgkurz fürMikrogramm/kgkurz fürKilogramm Lebensmittel für Naphthol AS beobachtet. Die toxikologische Datenlage ist aktuell nicht ausreichend, um diese Migration gesundheitlich bewerten zu können. Das BfRkurz fürBundesinstitut für Risikobewertung empfiehlt entsprechend, dass kein Übergang von Naphthol AS (sowie von NAAX und NDPA) oberhalb von 50 µgkurz fürMikrogramm/kgkurz fürKilogramm Lebensmittel stattfinden sollte. Die Hersteller sollten ihre Rohstoffe und Endprodukte auf Verunreinigungen mit diesen Substanzen bzw. deren Freisetzung prüfen und ggf. Alternativen zu den verwendeten Materialien suchen.
3 Begründung
3.1 Risikobewertung
3.1.1 Gefahrenidentifizierung
3.1.1.1 Mögliche Gefahrenquellen
Bei der Produktion von Papier und Karton, die zu verschiedenen Lebensmittelbedarfsgegenständen weiterverarbeitet werden sollen, wird eine Vielzahl von Hilfs- und Veredelungsstoffen eingesetzt, um die für die jeweilige Anwendung gewünschten Eigenschaften zu erzeugen. Die vier Stoffe Naphthol AS, HNS, NAAX und NDPA sind sehr wahrscheinlich der Gruppe der Ausgangsstoffe, Verunreinigungen oder Abbauprodukte von (Azo-) Farbmitteln zuzuordnen. Darauf deuten die Listung von NAAX und 2-Naphthol im Anhang 10 zu Druckfarben der Schweizer Bedarfsgegenständeverordnung (EDI 2017) sowie die chemische Struktur der vier Verbindungen hin.
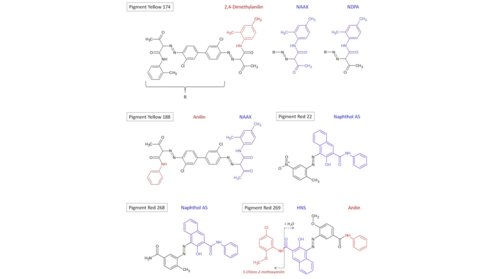
So enthalten beispielsweise die Pigmente Yellow 174 (CAS 78952-72-4), Yellow 188 (CAS 23792-68-9), Red 22 (CAS 6448-95-9), Red 268 (CAS 16403-84-2) oder Red 269 (CAS 67990-05-0) eine oder mehrere der vier oben genannten Verbindungen als Substrukturen (vgl. Abbildung 2). Die genannten Pigmente sind auch im Anhang 10 der Schweizer Bedarfsgegenständeverordnung (EDI, 2017) sowie zum Teil in Anlage 14 der deutschen Bedarfsgegenständeverordnung gelistet.
Über Naphthol AS, NAAX, NDPA und HNS hinaus wurden in den Kaltwasserextrakten einiger untersuchter Proben auch die Verbindungen Anilin (CAS 62-53-3), 2,4-Dimethylanilin (CAS 95-68-1) und 5-Chloro-2-methoxyanilin (CAS 95-03-4) bestimmt, die ebenfalls zu erwartenden Spaltprodukten oder Verunreinigungen einiger der in Abbildung 2 gezeigten Pigmente bzw. von Naphthol AS, NAAX und NDPA darstellen. Die genannten Abbauprodukte oder Verunreinigungen von Farbstoffen oder Pigmenten können im Kontakt mit Lebensmitteln auf diese übergehen und durch den Verbraucher oral aufgenommen werden.
3.1.2 Gefahrencharakterisierung
3.1.2.1 Aufnahme, Verteilung, Metabolismus, Exkretion (Ausscheidung)
Dem BfRkurz fürBundesinstitut für Risikobewertung liegen zu keiner der vier Verbindungen toxikokinetische Daten vor. Zur theoretischen Abschätzung einer möglichen Resorption der Verbindungen kann die „Rule of five“ (Lipinski et al.kurz füret alii (lat. "und andere") 2001) verwendet werden. Nach dieser Regel weisen gut resorbierbare Stoffe eine Molmasse von kleiner 500 g/mol und nicht mehr als fünf Wasserstoffbrückendonatoren, nicht mehr als zehn Wasserstoffbrückenakzeptoren sowie einen Octanol/Wasser-Verteilungskoeffizienten (LogPOW) ungefähr zwischen 0 und 5 auf. Dies trifft auf alle vier betrachteten Verbindungen zu (siehe Tabelle 1).
Tabelle 1: Strukturelle und physikochemische Daten zur Abschätzung der oralen Resorption entsprechend der „Rule of five“
| Naphthol AS | HNS | NAAX | NDPA | |
| Molmasse in g/mol | 263,3 | 188,2 | 205,3 | 163,2 |
| Anzahl Wasserstoffbrücken-Donatoren | 2 | 2 | 1 | 1 |
| Anzahl Wasserstoffbrücken-Akzeptoren | 1 | 1 | 2 | 1 |
| LogPOW* | 3,36 | 2,11 | 2,06 | 2,03 |
*Berechnet mit: Externer Link:http://www.swissadme.ch/index.php
Da zudem in der Literatur für jeden der Stoffe oder für chemisch/strukturell ähnliche Verbindungen in verschiedenen Studien systemische Toxizität berichtet wird (siehe unten), ist davon auszugehen, dass alle vier Verbindungen in relevanten Mengen über den Magen-Darm-Trakt ins Blut resorbiert werden. Für Naphthol AS, NAAX und NDPA ist die Frage der Metabolisierung und damit verbundenen Spaltung der Amidbindung von großer Bedeutung, da auf diesem Wege die primären aromatischen Amine Anilin bzw. 2,4-Dimethylanilin gebildet werden könnten. Anilin ist entsprechend VO (EG) Nr. 1272/2008 als mutagen und karzinogen der Klasse 2 eingestuft. 2,4-Dimethylanilin steht ebenfalls im Verdacht, mutagen und karzinogen (BAuA 2016) zu sein (siehe unten).
Naphthol AS: Nach der in silico-Vorhersage des Metabolismus mit Hilfe der OECD-Toolbox Version 4.6 tritt keine Spaltung der Amidbindung auf. Dass allerdings das Spaltprodukt HNS in einer Vielzahl von Proben gefunden wurde und zudem auch das Spaltprodukt Anilin in einer Probe nachgewiesen werden konnte (siehe Abschnitt 2 und 3.1.1), könnte darauf zurückzuführen sein, dass die Verbindung möglicherweise labil genug ist, um bereits in der technischen Anwendung oder danach gespalten zu werden. Die mögliche Spaltung von Naphthol AS in das primäre aromatische Amin Anilin nach oraler Aufnahme während der Verdauung wurde in zwei verschiedenen in vitro Modellen untersucht (Bittner et al.kurz füret alii (lat. "und andere") 2022). Ein Modell folgte den Empfehlungen der Europäischen Behörde für Lebensmittelsicherheit (EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit)), während das andere Modell vom Niederländischen Nationalen Institut für öffentliche Gesundheit und Umwelt (RIVM) entwickelt wurde. Das von der EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit) empfohlene Protokoll umfasst schärfere Bedingungen und eine längere Inkubationsdauer. Die beiden Modelle simulieren das aufeinanderfolgende Einwirken von Speichel, Magensaft und Darmflüssigkeit auf die Substanzen nach. Nach der Inkubation von Naphthol AS in beiden Verdauungsmodellen wurden mögliche Spaltprodukte mittels LC-MS/MS analysiert. Vor Beginn des Experiments wurde für Napthol AS ein Gehalt von 0,09 % Anilin als Verunreinigung gemessen. Über dieses Hintergrundniveau hinaus wurde weder im EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit) Modell noch im RIVM Modell ein Anstieg der Anilinkonzentration beobachtet. Daraus lässt sich schlussfolgern, dass unter den gewählten Bedingungen keine nachweisbare Hydrolyse von Naphthol AS zu Anilin stattfindet.
NAAX: Invivo wurde nach oraler Verabreichung von NAAX an Ratten die Bildung von 2,4-Dimethylanilin und dessen Bindung an Hämoglobinmoleküle im Blut der Ratten beobachtet (BUA 1992; Sabbioni 1999). Eine Aussage zur Metabolisierungsrate lässt die Studie jedoch nicht zu. Mit Hilfe der OECD-Toolbox Version 4.6 generierte in silico-Daten stützen den in vivo-Befund, da 2,4-Dimethylanilin als ein möglicher Metabolit vorhergesagt wird. In einer Arbeit von Rasper (2016) wurde zudem gezeigt, dass NAAX bei 80 °Ckurz fürGrad Celsius bereits in wässriger Lösung – ohne enzymatische Einwirkung – gespalten wird und das umso mehr, je niedriger der pH-Wert der Lösung ist. Das bei dieser Spaltung entstehende 2,4-Dimethylanilin wurde von der LUA Sachsen in 2 Proben zusätzlich zu NAAX nachgewiesen (siehe Abschnitt 2 und 3.1.1).
Zudem wurde in einer aktuellen Studie in vitro Verdauungsmodelle eingesetzt, um die mögliche Spaltung von NAAX zu 2,4-DMA zu untersuchen (Bittner et al.kurz füret alii (lat. "und andere") 2022). Zu diesem Zweck wurden, wie oben beschrieben, zwei unterschiedliche in vitro Verdauungsmodelle eingesetzt, und zwar eines von der EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit) und das andere von RIVM. Das Verdauungsmodell der EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit) zeigte, dass NAAX sowohl im Speichel als auch im Magensaft zu 2,4-DMA gespalten wurde, nicht jedoch in Darmflüssigkeit. Die höchste Spaltungsrate, 0,053 %, trat im Magensaft-Simulanz nach 4 Stunden Inkubation auf. Das vom RIVM erstellte in vitro Verdauungsmodell hingegen zeigte die Spaltung von NAAX in 2,4-DMA in allen drei Verdauungssimulanzien, allerdings mit geringeren Raten. Die maximale Hydrolyserate lag bei 0,033 %. Beide Modelle zeigen also eine sehr geringe Spaltung von NAAX zu 2,4-DMA, die leicht unterschiedlichen Ergebnisse sind wahrscheinlich auf die leicht verschiedenen Zusammensetzungen und pH-Werte der Simulanzien in den beiden in vitro Verdauungsmodellen zurückzuführen.
NDPA: Die Spaltung von Arylacetamiden wie NDPA kann in vivo durch das Enzym Arylacetamid-Deacetylase (AADAC) katalysiert werden (Fukami et al.kurz füret alii (lat. "und andere") 2015; Yoshida et al.kurz füret alii (lat. "und andere") 2018). Die Reaktion ist beispielsweise für die dem NDPA strukturell sehr ähnlichen Arzneistoffe Indiplon, Flutamid und Phenacetin gut untersucht (Kobayashi et al.kurz füret alii (lat. "und andere") 2012; Shimizu et al.kurz füret alii (lat. "und andere") 2014; Watanabe et al.kurz füret alii (lat. "und andere") 2009). Da auch mit Hilfe der OECD-Toolbox Version 4.6 generierte in silico-Daten auf eine Spaltung der Amidbindung des NDPA hindeuten, ging das BfRkurz fürBundesinstitut für Risikobewertung in seiner ursprünglichen Risikobewertung davon aus, dass eine Freisetzung von 2,4-Dimethylanilin während der Metabolisierung von NDPA stattfindet. Zudem hatte die LUA Sachsen zusätzlich zu NDPA in 2 Proben 2,4-Dimethylanilin nachgewiesen (siehe Abschnitt 2 und 3.1.1), was ebenfalls auf eine mögliche Spaltung von NDPA hindeutete. In einer neueren Studie wurden zwei verschiedene in vitro Verdauungsmodelle zur Untersuchung der potenziellen Spaltung von NDPA zu 2,4-DMA verwendet (Bittner et al.kurz füret alii (lat. "und andere") 2022). In dem von der EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit) empfohlenen Verdauungsmodell zeigte sich ein zeitabhängiger Anstieg von 2,4-DMA nach der Inkubation mit Magensaft-Simulanz, wobei die höchste Rate bei 0,21 % nach 4 Stunden Inkubation lag. Im Gegensatz dazu wurde in Speichel- und Darmflüssigkeitssimulanzien eine geringe oder gar keine Spaltung (<0,02 %) beobachtet. In Übereinstimmung mit diesen Ergebnissen wurde auch bei dem vom RIVM erstellten in vitro Verdauungsmodell eine Bildung von 2,4-DMA hauptsächlich nach der Inkubation mit Magensaft-Simulanz beobachtet (Maximum: 0,021 % nach 4 Stunden), während die anschließende Inkubation mit einem Darmflüssigkeitssimulanz zu keinem weiteren Anstieg an 2,4-DMA führte. Arylacetamid-Deacetylase (AADAC) war in dem Enzymmix nicht enthalten, weshalb eine Unsicherheit bestehen bleibt, ob NDPA in vivo in der Leber nicht doch gespalten werden könnte.
3.1.2.2 Genotoxitität / Kanzerogenität
Außer für NDPA liegen dem BfRkurz fürBundesinstitut für Risikobewertung zu keiner der vier Verbindungen vollständige Originaldaten vor. Keine der Verbindungen wurde entsprechend Verordnung (EG) Nr. 1272/2008 (CLP) harmonisiert eingestuft. Zudem wurde für keine der Verbindungen eine Karzinogenitätsstudie, beispielsweise entsprechend nach OECD Richtlinie 451, durchgeführt. Für NAAX und HNS liegen Zusammenfassungen von Studien zur Genotoxizität vor. Für NDPA liegen zwei in vitro Tests entsprechend der OECD Richtlinien zur Genotoxizität vor. Das BfRkurz fürBundesinstitut für Risikobewertung hat zudem mit Hilfe der OECD-Toolbox Version 4.6 sowie der Algorithmen „Derek Nexus“ (Version 1.1) sowie „Sarah Nexus“ (Version 2.0) in silico Vorhersagen zur Genotoxizität und Karzinogenität erstellt sowie Möglichkeiten eines „Read-across“ zu strukturell ähnlichen Verbindungen erwogen. Nachfolgend sind die vorhandenen Daten und die Ergebnisse der Vorhersagen bzw. des „Read-across“ dargestellt.
3.1.2.3 Studiendaten
NDPA: Es liegen zwei in vitro Studien zur Genotoxizität vor: ein Mutagenitätstest in Bakterien (Ames-Test, entsprechend OECD Richtlinie 471) und ein in vitro Mikrokern-Test (entsprechend OECD Richtlinie 487). NDPA verursachte unabhängig von der Stoffwechselaktivität keine Veränderung der Anzahl der Revertantenkolonien. Ebenso hat NDPA sowohl mit als auch ohne metabolische Aktivierung nicht zu einer Erhöhung der Anzahl mikrokernhaltiger humaner Lymphozyten geführt. NDPA zeigte unter den Testbedingungen keine genotoxischen Wirkungen und Studien wurden entsprechend der Richtlinien durchgeführt.
Naphthol AS: Es liegen zwei japanische Studien zur Genotoxizität vor: ein Mutagenitätstest in Bakterien (Ames-Test) und ein in vitro-Chromosomenaberrationstest (JECDB 2019a). Aus den englischsprachigen Ergebnistabellen geht hervor, dass die Substanz als in vitro nicht genotoxisch zu bewerten ist. Ob alle Vorgaben der entsprechenden OECD-Richtlinie 471 bzw. 473 eingehalten wurden, ist aus den englischsprachigen Ergebnistabellen nicht ersichtlich. In vivo Untersuchungen zur Genotoxizität liegen nicht vor.
NAAX: Im bei der ECHAkurz fürEuropäische Chemikalienagentur vorliegenden Registrierungsdossier (ECHAkurz fürEuropäische Chemikalienagentur 2019g) sind eine Studie zur Mutagenität in Bakterien entsprechend OECD Richtlinie 471 (Ames-Test) und ein in vitro-Chromosomenaberrationstest entsprechend OECD Richtlinie 473 aufgeführt. Die Studien wurden von den Registranden als valide und entsprechend der Richtlinien durchgeführt eingestuft. Bei beiden Studien wurde sowohl mit als auch ohne metabolische Aktivierung keine genotoxische Wirkung von NAAX beobachtet. Diese Einschätzung wird auch durch das „Beratergremium für umweltrelevante Altstoffe“ der Gesellschaft Deutschscher Chemiker (GDCh) geteilt (BUA 1992). Allerdings ist nicht klar, ob die Testbedingungen und der eingesetzte Enzym Mix (S9) aus der Rattenleber geeignet sind, eine mögliche Abspaltung von 2,4-Dimethylanilin aus NAAX in vivo zu modellieren.
HNS: Im bei der ECHAkurz fürEuropäische Chemikalienagentur vorliegenden Registrierungsdossier (ECHAkurz fürEuropäische Chemikalienagentur 2019i) sind eine Studie zur Mutagenität in Bakterien entsprechend OECD Richtlinie 471 (Ames-Test), ein in vitro Chromosomenaberrationstest entsprechend OECD Richtlinie 473 und ein in vivo Chromosomenaberrationstest entsprechend OECD Richtlinie 475 an Hamstern nach oraler Verabreichung der Substanz aufgeführt. Die Studien wurden von den Registranden als valide und entsprechend der Richtlinien durchgeführt eingestuft. Als Einschränkung ist beschrieben, dass bei dem in vivo Chromosomenaberrationstest nur sehr wenige Zellen untersucht wurden. Die Substanz wurde als nicht genotoxisch im Ames-Test, jedoch als genotoxisch im in vitro Chromosomenaberrationstest (ohne metabolische Aktivierung) bewertet. Dieser Bewertung schloss sich auch die OECD an (OECD 2004). In vivo zeigte HNS keine genotoxischen Eigenschaften. Allerdings ist die Validität der Studie aufgrund der geringen Anzahl untersuchter Zellen sehr eingeschränkt. Zusätzlich ist in der Literatur ein in vivo Mikrokerntest entsprechend OECD Richtlinie 474 beschrieben (JECDB). Der Studienbericht ist in japanischer Sprache verfasst, die Ergebnistabellen sowie eine Zusammenfassung liegen in englischer Sprache vor. Demnach ist HNS als nicht genotoxisch zu bewerten. Aus den englischen Passagen ist nicht ersichtlich, ob die Vorgaben der OECD Richtlinie 474 eingehalten wurden. Daher wurde die aus der Studie extrahierbare japanische Zusammenfassung übersetzt. Die Autoren berichten im methodischen Teil, dass pro Tier 2000 polychromatische Erythrozyten untersucht wurden, was der Vorgabe aus der OECD Richtlinie 474 entspricht.
In silico-Daten
In der Tabelle 2 sind die mittels der OECD-Toolbox Version 4.6 sowie die mittels der Algorithmen „Derek Nexus“ (Version 6.3) und „Sarah Nexus“ (Version 3.3) erzeugten Vorhersagen zur Genotoxizität / Kanzerogenität inklusive der jeweiligen Begründung darge-stellt. Dabei wird deutlich, dass bis auf HNS alle Verbindungen aufgrund ihrer chemischen Struktur ein Potential zur Bindung an Proteine aufweisen, aber nicht an die DNA. Die im Abschnitt 3.1.2.1 diskutierte Freisetzung von Anilinderivaten wird auch durch die in silico-Vorhersagen als möglich eingestuft. Für HNS ist nur die Vorhersage, dass die Verbindung zur Bildung von Mikronuklei bzw. Chromosomenaberrationen führen könnte, positiv, was der Vorhersagealgorithmus mit dem Vorliegen einer chinoiden Struktur und der Möglichkeit einer Addition eines Nukleophils an eine α,β-ungesättigte Carbonylverbindung begründet (Michael-Addition). Beides scheint nichtzutreffend, da die Verbindung keine chinoide Struktur aufweist und die Michael-Addition zur Aufhebung der Aromatizität führen würde und damit energetisch ungünstig wäre. Somit ist dieser alert als nichtzutreffend zu bewerten. Für Naphtol AS lagen überwiegend negative Ergebnisse vor mit Ausnahme von Sarah Nexus, dass ein positives Ergebnis mit einer niedrigen Sicherheit zeigte. Zusammenfassend gibt es keinen starken Hinweis auf eine Genotoxizität von Naphtol AS. Bei NAAX weist Derek Nexus auf ein mögliches Risiko hin (aromatische Amine), Sarah Nexus liefert jedoch ein negatives Ergebnis. Insgesamt geben die verschiedenen Tools gegensätzliche Ergebnisse, ein klarer Concern für Genotoxizität lässt sich daraus nicht ableiten. Für NDPA zeigen sich konsistente Strukturalerts bei Derek Nexus und der OECD Toolbox hinsichtlich einer möglichen Genotoxizität durch aromatische Amine. Insgesamt weist NDPA das höchste Risiko im Vergleich der untersuchten Substanzen auf.
Tabelle 2: Zusammenfassung der generierten in silico-Daten
| Programm / Algorithmus | Naphthol AS | HNS | NAAX | NDPA |
| Derek Nexus | ||||
| Karzinogenität | kein alert | kein alert | plausibel, aromatisches Amin oder Amid | plausibel, aromatisches Amin oder Amid, Anilin / Vorläufer |
| Chromosomenschädigung in vitro | kein alert | kein alert | uneindeutig, Anilin/ Alkylanilin | uneindeutig, Anilin/ Alkylanilin |
| Mutagenität in vitro | negativ | negativ | plausibel, aromatisches Amin oder Amid | plausibel, aromatisches Amin oder Amid |
| Mutagenität in vivo | kein alert | kein alert | uneindeutig, aromatisches Amin oder Amid | uneindeutig, aromatisches Amin oder Amid |
| Sarah Nexus | ||||
| Mutagenität in vitro | positiv, 11 % Sicherheit | negativ, 29 % Sicherheit | negativ, 100 % Sicherheit | equivocal |
| OECD Toolbox | ||||
| Bindung an DNA | nein | nein | nein | nein |
| Bindung an Proteine | ja, Acylierung | nein | ja, Acylierung | ja, Acylierung |
| Karzinogenität | nein | nein | nein | ja, aromatisches N-Acylamin (Genotoxizität) |
| in vitro Mutagenität (Ames) | nein | nein | nein | ja, aromatisches N-Acylamin |
| in vitro / in vivo Genotoxizität (Mikronukleus / Chromosomenaberration) | ja, H-Akzeptor | ja, H-Akzeptor | ja, H-Akzeptor | ja, aromatisches N-Acylamin |
Read-across
Naphthol AS: Für die strukturell sehr ähnlichen Verbindungen 1, 2, 3 und 4 in Abbildung 3 ist im jeweiligen Registrierungsdossier der ECHAkurz fürEuropäische Chemikalienagentur (ECHAkurz fürEuropäische Chemikalienagentur 2019b; ECHAkurz fürEuropäische Chemikalienagentur 2019c; ECHAkurz fürEuropäische Chemikalienagentur 2019e; ECHAkurz fürEuropäische Chemikalienagentur 2019j) jeweils ein Ames-Test entsprechend OECD Richtlinie 471 angegeben. Für die Verbindung 2 ist zudem ein in vivo Mikrokerntest entsprechend OECD Richtlinie 474 aufgeführt. Da dem BfRkurz fürBundesinstitut für Risikobewertung die Originaldaten nicht vorliegen, kann das BfRkurz fürBundesinstitut für Risikobewertung nicht überprüfen, ob die Vorgaben der Richtlinien – beispielsweise bezüglich verwendender Bakterienstämme im Ames-Test oder der Anzahl an untersuchten Zellen – eingehalten wurden. Von den jeweiligen Registranden werden die Studien als valide eingeschätzt. In allen Tests wurde die getestete Substanz als nicht genotoxisch eingestuft.
Ein Read-across zum Naphthol AS scheint auf der Grundlage der vorliegenden Daten möglich. Naphthol AS selbst kann folglich als nicht genotoxisch angesehen werden. Ob Naphthol AS jedoch möglicherweise in vivo gespalten wird und das genotoxische Kanzerogen Anilin (siehe unten) freisetzt, kann auf der Grundlage der Daten nicht evaluiert werden. Es wurde bei dem in vivo Mikrokerntest von Verbindung 2 an Ratten keine Genotoxizität beobachtet, obwohl auch dort die Freisetzung eines Anilins möglich ist. Allerdings wird bei einer möglichen Spaltung der Verbindung 2 zunächst 2-Ethoxyanilin freigesetzt, welches im Gegensatz zum Anilin nicht harmonisiert als mutagen oder kanzerogen eingestuft ist. Darüber hinaus liegen keine Informationen dazu vor, ob Naphthol AS und Verbindung 2 tatsächlich gleichermaßen metabolisiert werden.
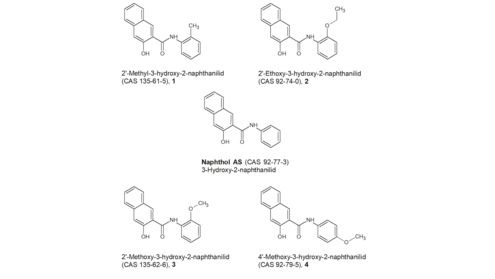
NAAX: Für die strukturell sehr ähnlichen Verbindungen 1 (ECHAkurz fürEuropäische Chemikalienagentur 2019l), 2 (ECHAkurz fürEuropäische Chemikalienagentur 2019f; JECDB 2019b), 3 (Toxnet) und 4 (ECHAkurz fürEuropäische Chemikalienagentur 2019d) in Abbildung 4 sind verschiedene in vitro Genotoxizitätstests durchgeführt worden, darunter für alle Verbindungen ein Ames-Test entsprechend OECD Richtlinie 471. Für die Verbindungen 1 und 2 wurden zudem in vitro Chromosomenaberrationstests entsprechend OECD Richtlinie 473 sowie für die Verbindungen 2 und 4 Genmutationsstudien in Säugerzellen entsprechend OECD Richtlinie 476 durchgeführt. Da dem BfRkurz fürBundesinstitut für Risikobewertung die Originaldaten nicht vorliegen, kann das BfRkurz fürBundesinstitut für Risikobewertung auch für diese Studien nicht überprüfen, ob die Vorgaben der Richtlinien eingehalten wurden.
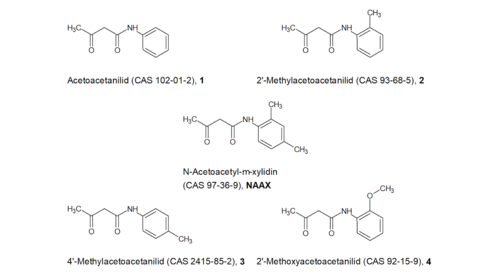
Trotz vereinzelter positiver Ergebnisse (denen jedoch in Wiederholungstests stets negative Ergebnisse gegenüberstanden) sind die Verbindungen insgesamt als nicht genotoxisch in vitro anzusehen. Die Ergebnisse der Genotoxizitätstests für NAAX (siehe oben) werden damit bestätigt. Ob NAAX jedoch möglicherweise in vivo gespalten wird und das möglicherweise genotoxische und möglicherweise kanzerogene 2,4-Dimethylanilin (siehe unten) freisetzt, kann auf der Grundlage der in vitro Daten nicht evaluiert werden.
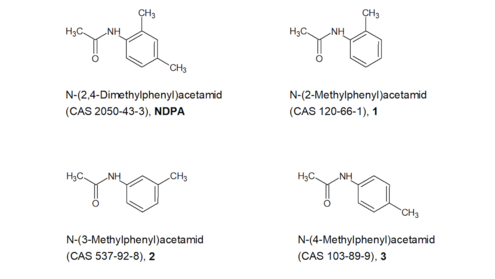
NDPA: Für die strukturell sehr ähnliche Verbindung 2 in Abbildung 5 ist in der Literatur ein negativer Ames-Test entsprechend OECD Richtlinie 471 publiziert (Zeiger et al.kurz füret alii (lat. "und andere") 1992). Der Ames-Test zu Verbindung 3 in Abbildung 5 war hingegen schwach positiv (Zeiger et al.kurz füret alii (lat. "und andere") 1992). Für Verbindung 1 in Abbildung 5 weist die OECD Toolbox Version 4.1 einen negativen Ames-Test aus, der in der OASIS-Genotoxizitätsdatenbank hinterlegt ist. Das BfRkurz fürBundesinstitut für Risikobewertung hat keinen Zugriff auf die Originaldaten. Die Einhaltung der Vorgaben der OECD Richtlinie 471 kann entsprechend nicht überprüft werden. Tests zu den clastogenen oder aneugenen Eigenschaften der Verbindungen liegen nicht vor. Ob die Verbindungen 1-3 genotoxisch sind, kann daher auf Basis dieser Daten nicht abschließend beurteilt werden. Für NDPA selbst liegen zwei neue Genotoxizitätstests vor (siehe oben), die konform mit der jeweiligen OECD Richtlinie und negativ sind.
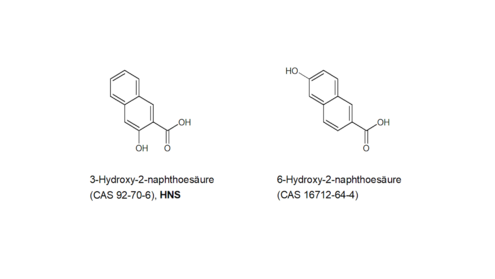
HNS: Für die strukturell sehr ähnliche Substanz 6-Hydroxy-2-naphthoesäure (CAS 16712-64-4, Abbildung 6) sind im Registrierungsdossier der ECHAkurz fürEuropäische Chemikalienagentur (ECHAkurz fürEuropäische Chemikalienagentur 2019k) – analog zu HNS – ein positiver in vitro-Chromosomenaberrationstest sowie ein negativer in vivo Mikrokerntest angegeben. In der Testzusammenfassung der in vivo-Studie ist angegeben, dass je Tier 2000 Erythrozyten auf Mikrokerne untersucht wurden. Da dem BfRkurz fürBundesinstitut für Risikobewertung die Originaldaten nicht vorliegen, können die Angaben vom BfRkurz fürBundesinstitut für Risikobewertung nicht überprüft werden.
Ein Read-across von HNS zu 6-Hydroxy-2-naphthoesäure ist aufgrund der chemisch / strukturellen Ähnlichkeit möglich. HNS ist damit als in vivo nicht genotoxisch anzusehen.
3.1.2.4 Sonstige Toxizität
Naphthol AS: Es liegt eine japanische Screening-Studie an SD-Ratten zur kombinierten Toxizität nach wiederholter Aufnahme und zur Reproduktionstoxizität nach OECD-Richtlinie 422 vor (JCHECK 2019). Dabei wurden über einen Zeitraum von 42 Tagen Dosen von 0, 40, 200 und 1000 mgkurz fürMilligramm/kgkurz fürKilogramm Körpergewicht (KG)/Tag per Schlundsonde verabreicht. Aus den englischsprachigen Ergebnistabellen geht hervor, dass – bis auf wenige Abweichungen bei einigen Laborparametern (Chlorid, Phosphat) in der höchsten Dosis – keine Effekte beobachtet wurden. Die Dosis, bei der keine adversen Effekte beobachtet wurden (NOAEL), betrug 1000 mgkurz fürMilligramm/kgkurz fürKilogramm KG/Tag (höchste Dosis). Eine Screening-Studie stellt jedoch lediglich einen ersten Hinweis auf eventuelle Effekte bei lebenslanger ExpositionExpositionZum Glossareintrag dar und kann eine subchronische oder chronische Studie nicht ersetzen. Die Ableitung einer duldbaren täglichen Aufnahmemenge (TDIkurz fürTolerable Daily Intake (tolerierbare tägliche Aufnahmemenge)) ist daher auf der Grundlage der vorliegenden Daten nicht möglich.
NAAX: Es liegt eine japanische Screening-Studie an Sprague-Dawley-Ratten zur kombinierten Toxizität nach wiederholter Aufnahme und zur Reproduktionstoxizität nach OECD Richtlinie 422 vor (ECHAkurz fürEuropäische Chemikalienagentur 2019f; JECDB 2019b). Dabei wurden über einen Zeitraum von 44 Tagen Dosen von 0, 8, 25, 80 und 250 mgkurz fürMilligramm/kgkurz fürKilogramm Körpergewicht (KG)/Tag per Schlundsonde verabreicht. Es wurden folgende Effekte beobachtet: Anzeichen einer Methämoglobinämie in den beiden höchsten Dosisgruppen (verringerte Erythrozytenzahl, Hämoglobinkonzentration und Hämatokritwerte sowie erhöhte Methämoglobinwerte), wie sie typisch sind bei einer Exposition gegenüber Anilinderivaten (Kobayashi et al.kurz füret alii (lat. "und andere") 2012); Nekrosen in der Milz sowie erhöhte Milzgewichte, Ablagerungen von Hämosiderin in der Leber und von eosinophilen Blutkörperchen in der Niere in den beiden höchsten Dosisgruppen. Der NOAEL betrug 25 mgkurz fürMilligramm/kgkurz fürKilogramm KG/Tag. Eine Screening-Studie stellt jedoch lediglich einen ersten Hinweis auf eventuelle Effekte bei lebenslanger Exposition dar und kann eine subchronische oder chronische Studie nicht ersetzen. Die Ableitung eines TDIkurz fürTolerable Daily Intake (tolerierbare tägliche Aufnahmemenge) ist daher auf der Grundlage der vorliegenden Daten nicht möglich.
NDPA: Es liegen dem BfRkurz fürBundesinstitut für Risikobewertung keine Studien nach wiederholter Aufnahme vor. Wie im Abschnitt 3.1.2. dargestellt, ist eine Spaltung der Verbindung im Magen-Darm-Trakt zu erwarten. Vor kurzem publizierte Daten (siehe oben) zeigen eine nur sehr geringe Spaltung von NDPA in Verdauungssimulanzien.
HNS: Im Registrierungsdossier der ECHAkurz fürEuropäische Chemikalienagentur (ECHAkurz fürEuropäische Chemikalienagentur 2019i) sind eine subchronische Studie an Ratten entsprechend OECD Richtlinie 407 und eine Eingenerationenstudie an Ratten zur Reproduktionstoxizität entsprechend OECD Richtlinie 415 angegeben. Originaldaten liegen nur für letztere in japanischer Sprache mit englischsprachigen Ergebnistabellen vor (JECDB 2000) . Beide Studien wurden auch von der OECD bewertet (OECD 2004). In der subakuten Studie wurden erniedrigte Serum-Phosphat-Konzentrationen und erhöhte Bilirubinkonzentrationen im Serum und Urin beider Geschlechter festgestellt. Die Weibchen wiesen zudem leicht erhöhte Lebergewichte in der höchsten Dosis, sowie bei je einem Tier der höchsten und mittleren Dosisgruppe, eine Nekrose der Nebenniere auf. Als NOAEL wurde demnach die niedrigste Dosis von 12 mgkurz fürMilligramm/kgkurz fürKilogramm KG/Tag angesehen. In der Eingenerationenstudie wurde der Elterngeneration (F0) vor der Verpaarung, während der Trächtigkeit und danach insgesamt 98 Tage lang HNS per Schlundsonde zugeführt. Dabei wurde auf Auswirkungen auf den Nachwuchs (F1), aber auch auf adverse Effekte bei der F0 hin untersucht. Der einzige für den Nachwuchs beobachtete Effekt war ein reduziertes mittleres Körpergewicht in der höchsten Dosisgruppe (200 mgkurz fürMilligramm/kgkurz fürKilogramm KG/Tag). In der F0 Generation wurden in der Hochdosisgruppe vereinzelt Lebervergrößerungen beobachtet. Zudem zeigte die histologische Untersuchung Hyperplasien der Schleimhaut des Vormagens. Der NOAEL betrug 12,5 mgkurz fürMilligramm/kgkurz fürKilogramm KG/Tag. Eine Reihe von Informationen, beispielsweise zu einzelnen Organgewichten sowie Urin- und Blutparametern, wie sie für eine subchronische Studie entsprechend OECD Richtlinie 408 vorgeschrieben sind, sind in der vorliegenden Studie nicht dokumentiert. Einige wichtige Informationen zur Bewertung der Toxizität nach wiederholter Aufnahme fehlen demnach.
Anilinderivate: Wie im Abschnitt 3.1.2.1. beschrieben, können bei oraler Aufnahme von Naphthol AS, NAAX und NDPA durch deren Spaltung möglicherweise Anilin bzw. 2,4-Dimethylanilin freigesetzt werden. In Verdauungssimulanzien wurde jedoch nur ein sehr geringer Anteil der Substanzen tatsächlich gespalten.
- Anilin: Anilin ist entsprechend der Verordnung (EG) Nr. 1272/2008 (CLP) als Mutagen (Klasse 2, „kann vermutlich genetische Defekte verursachen“) und Karzinogen (Klasse 2, „kann vermutlich Krebs erzeugen“) eingestuft. Im Ames-Test wurde Anilin zwar als nicht genotoxisch getestet, allerdings liegen positive Mutagenitätstests an Säugerzellen sowie positive in vitro Mikrokern- und Chromosomenaberrationstests vor (ECHAkurz fürEuropäische Chemikalienagentur 2019m; EU 2004). In vivo waren die Ergebnisse nicht eindeutig. In Mäusen wurden clastogene Effekte nicht oder nur bei sehr hohen, systemisch toxischen Dosen beobachtet; bei Ratten hingegen traten diese Effekte auch bei deutlich niedrigeren Dosen auf (ECHAkurz fürEuropäische Chemikalienagentur 2019m; EU 2004). Im gleichen Maße unterschieden sich die Ergebnisse der Tierstudien auch in Hinblick auf Karzinogenität. So konnte an Mäusen keine karzinogene Wirkung nachgewiesen werden, während an Ratten die Bildung von Sarkomen der Milz beobachtet wurde (ECHAkurz fürEuropäische Chemikalienagentur 2019m; EU 2004). Beim Menschen wird Anilin schon seit dem 19. Jahrhunderts als Auslöser für Blasenkrebs diskutiert. Auch in modernen Studien wurde bei Arbeitern, die verschiedenen Chemikalien, unter anderem Anilin, ausgesetzt waren, ein erhöhtes Auftreten von Blasenkrebs nachgewiesen. Der Effekt konnte aber nicht eindeutig dem Anilin zugeordnet werden (EU 2004).
- 2,4-Dimethylanilin (DMA): DMA ist nicht harmonisiert eingestuft. Im Registrierungsdossier der ECHAkurz fürEuropäische Chemikalienagentur sind zwei positive in vitro-Chromosomenaberrationstests sowie positive Ames-Tests angegeben (ECHAkurz fürEuropäische Chemikalienagentur 2019h). In vivo-Daten zur Mutagenität sind dem BfRkurz fürBundesinstitut für Risikobewertung nicht bekannt. Zur Karzinogenität ist bei der ECHAkurz fürEuropäische Chemikalienagentur eine 18-Monatsstudie an Mäusen und Ratten angegeben. Für keine der Studien liegen dem BfRkurz fürBundesinstitut für Risikobewertung die Originaldaten vor. Die Karzinogenitätsstudie ist nicht unter GLP und mit einigen Abweichungen zur entsprechenden OECD Richtlinie 451 durchgeführt worden. So wurden beispielsweise nur zwei Dosisgruppen und bei den Ratten nur die Männchen untersucht. Auffälligkeiten zeigten sich nur bei den weiblichen Mäusen. In der Hochdosisgruppe (250 mgkurz fürMilligramm/kgkurz fürKilogramm KG/Tag) war die InzidenzInzidenzZum Glossareintrag für Lungentumore im Vergleich zur Kontrolle signifikant erhöht. Da der entsprechende Mausstamm (CD-1) bekannt ist, auch spontan diese Krebsform auszubilden, ist fraglich, ob die Ergebnisse auf den Menschen übertragbar sind. Bis zum Vorliegen entsprechender in vivo-Studien muss aber zumindest davon ausgegangen werden, dass DMA möglicherweise genotoxisch ist, zumal die strukturell sehr ähnliche Verbindung 2,6-Dimethylanilin harmonisiert als Karzinogen (Klasse 2, „kann vermutlich Krebs erzeugen“) eingestuft ist (ECHAkurz fürEuropäische Chemikalienagentur 2019a).
3.1.2.5 Zusammenfassung und Ableitung gesundheitlich akzeptabler Aufnahmemengen
Naphthol AS: Aus den vorliegenden experimentellen Daten lässt sich schließen, dass Naphthol AS in vitro nicht genotoxisch ist. Die in silico-Daten deuten zwar auf ein gewisses Potential zur Bindung an DNA und Proteine hin, doch bei Studien (inklusive in vivo-Studien) an chemisch / strukturell ähnlichen Verbindungen wurde kein Hinweis auf Genotoxizität gefunden. In einer Screening-Studie zur Toxizität nach wiederholter Aufnahme und zur Reproduktionstoxizität traten auch in der höchsten Dosisgruppe von 1000 mgkurz fürMilligramm/kgkurz fürKilogramm KG/Tag keine adversen Effekte auf. Umfassende Daten zur (sub)-chronischen Toxizität fehlen jedoch. In einer früheren Version dieser Stellungnahme wurde es jedoch als wahrscheinlich angesehen, dass im Magen-Darm-Trakt durch Spaltung der Amidbindung das genotoxische Kanzerogen Anilin freigesetzt wird. Dies wurde nun mithilfe eines in vitro Verdauungsmodell untersucht, und unter den angewendeten Testbedingungen konnte keine Hydrolyse von Naphthol AS nachgewiesen werden. Die Ergebnisse wurden durch zwei verschiedene Verdauungsmodells bestätigt, von denen eines dem von der EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit) empfohlenen Protokoll entspricht. Die NachweisgrenzeLimit of detectionZum Glossareintrag für Anilin im Magensimulanz liegt bei 0,9 ng/mlkurz fürMilliliter. Unter Anwendung dieses Wertes als Freisetzungsmenge für Anilin ergab sich eine maximale Spaltung von Naphthol AS von 0,023 %.
Auf Grundlage dieser Daten bewertet das BfRkurz fürBundesinstitut für Risikobewertung eine Freisetzung von Naphthol AS von bis zu 50 µgkurz fürMikrogramm/kgkurz fürKilogramm Lebensmittel als akzeptabel. Mit einer Spaltung von 0,023 % würde dies eine Bildung von maximal 0,012 µgkurz fürMikrogramm Anilin/kgkurz fürKilogramm Lebensmittel bedeuten.
Zudem haben wir das Margin of Exposure (MOEkurz fürMargin of Exposure) als Instrument für die Risikocharakterisierung angewendet. Basierend auf dem NOAEL von 1000 mgkurz fürMilligramm/kgkurz fürKilogramm KG/Tag aus der oben genannten Studie und der höchsten gemessenen Expositionswert von 274 µgkurz fürMikrogramm/Person/Tag sowie unter Anwendung eines Sicherheitsfaktors von 6 zur Extrapolation aus einer subakuten Studie, wurde ein MOEkurz fürMargin of Exposure von 36470 berechnet. Dieser MOEkurz fürMargin of Exposure-Wert deutet selbst bei der höchsten Exposition auf ein geringeres Risiko für Verbraucherinnen und Verbraucher hin.
NAAX: Aus den vorliegenden experimentellen Daten für NAAX und strukturähnliche Verbindungen lässt sich schließen, dass NAAX in vitro nicht genotoxisch ist. Die in silico-Daten sagen jedoch ein beträchtliches genotoxisches und kanzerogenes Potential für NAAX voraus, vor allem aufgrund seines Charakters als wahrscheinlicher Anilin-Vorläufer. Entsprechende in vivo-Metabolismusstudien weisen die Freisetzung von 2,4-Dimethylanilin und dessen anschließende Bindung an Hämoglobin nach. Auch eine Screening-Studie zur Toxizität nach wiederholter Aufnahme und zur Reproduktionstoxizität weist neben Effekten auf Leber, Niere und Milz typische Merkmale einer Methämoglobinämie nach, wie sie nach Bindung von Anilinderivaten an Hämoglobin auftreten kann. In einem in vitro Verdauungsmodell wurde die höchste Spaltungsrate von NAAX nach einer 4-stündigen Inkubation mit Magensaftsimulanz (0.07 M HCL) festgestellt und betrug 0.053% (Bittner et al.kurz füret alii (lat. "und andere") 2022). Angesichts der äußerst geringen Hydrolyserate der Amidbindungen von NAAX während der simulierten Magenpassage entstehen nur minimale Mengen des potenziell mutagenen aromatischen Amin 2,4-DMA. Auf Grundlage der vorliegenden Daten bewertet das BfRkurz fürBundesinstitut für Risikobewertung eine Freisetzung von NAAX von bis zu 50 µgkurz fürMikrogramm/kgkurz fürKilogramm Lebensmittel als akzeptabel. Mit einer Spaltung von 0,053 % würde dies eine Bildung von maximal 0,016 µgkurz fürMikrogramm 2,4-DMA/kgkurz fürKilogramm Lebensmittel bedeuten.
NDPA: Für diese Verbindung wurden zwei in vitro Genotoxizitätstests durchgeführt. Der Ames-Test, der gemäß den OECD 471 durchgeführt wurde, zeigte keine Zunahme der Revertantenkolonien, weder mit noch ohne metabolische Aktivierung. Ebenso zeigte der in vitro Mikrokerntest mit humanen Lymphozyten keine Erhöhung der Anzahl mikrokernhaltiger Zellen, ebenfalls weder mit noch ohne metabolische Aktivierung. Auf Grundlage dieser Ergebnisse wurde NDPA als nicht genotoxisch bewertet. Die in silico-Daten sagen jedoch ein erhebliches genotoxisches und kanzerogenes Potential für NDPA voraus – vor allem aufgrund seines Charakters als Anilin-Vorläufer, denn in vivo wird NDPA sehr wahrscheinlich zu 2,4-Dimethylanilin gespalten. Die Reaktion wird durch das Enzym Arylacetamid-Deacetylase katalysiert und ist für strukturverwandte Arzneistoffe gut beschrieben. Mithilfe eines in vitro Verdauungsmodells wurde die Hydrolyse von NDPA zu 2,4-Dimethylanilin untersucht (Bittner et al.kurz füret alii (lat. "und andere") 2022). Unter den angewendeten Testbedingungen konnte nur eine begrenzte Hydrolyse (maximal 0,21 %) festgestellt werden. Auf Grundlage der vorliegenden Daten bewertet das BfRkurz fürBundesinstitut für Risikobewertung eine Freisetzung von NAAX von bis zu 50 µgkurz fürMikrogramm/kgkurz fürKilogramm Lebensmittel als akzeptabel. Mit einer Spaltung von 0,21 % würde dies eine Bildung von maximal 0,078 µgkurz fürMikrogramm 2,4-DMA/kgkurz fürKilogramm Lebensmittel bedeuten.
HNS: Die Verbindung ist, wenn man alle experimentellen und in silico-Informationen zu ihr und chemisch / strukturell ähnlichen Verbindungen heranzieht, als nicht genotoxisch einzustufen. In Studien zur Toxizität nach wiederholter Aufnahme zeigten sich Effekte auf die Nebenniere und Hyperplasien der Vormagenschleimhaut. Der NOAEL betrug 12 mgkurz fürMilligramm/kgkurz fürKilogramm KG/Tag. Allerdings fehlt zu einer umfassenden Untersuchung der (sub) chronischen Toxizität eine Vielzahl an Daten beispielsweise zu den Organgewichten und den Blut- bzw. Urinwerten. Zur Ableitung einer tolerierbaren täglichen Aufnahmemenge (TDIkurz fürTolerable Daily Intake (tolerierbare tägliche Aufnahmemenge)) wird daher ein Gesamtunsicherheitsfaktor von 2000 herangezogen (je Faktor 10 für Inter- und Intraspezies-Unterschiede, Faktor 2 für die Extrapolation von einer subchronischen auf eine chronische Studie sowie Faktor 10 für Unsicherheiten in der Datenbasis). Der TDIkurz fürTolerable Daily Intake (tolerierbare tägliche Aufnahmemenge) beträgt demnach 6 µgkurz fürMikrogramm/kgkurz fürKilogramm KG/Tag. Für einen Erwachsenen (KG = 60 kgkurz fürKilogramm, tägliche Aufnahme von Lebensmittel, das im Kontakt mit dem betrachteten Material war = 1 kgkurz fürKilogramm) entspricht das einem gesundheitlich akzeptablen Aufnahmewert von 360 µgkurz fürMikrogramm/Tag.
Akzeptable Migrationswerte: Entsprechend der Verordnung (EU) Nr. 10/2011 wird für eine erwachsene Person eine tägliche Verzehrmenge von 1 kgkurz fürKilogramm Lebensmittel, das mit dem entsprechenden FCM in Kontakt war, angenommen. Akzeptable Migrationswerte (in µgkurz fürMikrogramm/l) entsprechen daher dem Zahlenwert nach den akzeptablen täglichen Aufnahmemengen (siehe Tabelle 3). Bei Verwendung des Kaltwasserextraktes als Migrationstest sind Konzentrationen an Naphthol AS, NAAX und NDPA von 50 µgkurz fürMikrogramm/l akzeptabel. Für HNS ist eine Migration von 360 µgkurz fürMikrogramm/l akzeptabel (siehe Tabelle 3).
Tabelle 3: Gesundheitlich akzeptable Aufnahmewerte und akzeptable Migrationswerte für den Wasserextrakt für Naphthol AS, NAAX, NDPA und HNS
| Naphthol AS | NAAX | NDPA | HNS | |
| Gesundheitlich akzeptable Aufnahmewerte in µg/Person/Tag | 50 | 50 | 50 | 360 |
| Akzeptable Migrationswerte in µg/l | 50 | 360 | ||
3.1.3 Expositionsschätzung und -bewertung
Aufgrund der Daten der LUA Sachsen (2018), welche im Rahmen der Analytik primärer aromatischer Amine auch die oben genannten Verbindungen (Abbildung 1) in Kaltwasserextrakten aus Papier- und Kartonmatrices bestimmt hat, ist ein Übergang der Verbindungen auf Lebensmittel bei Kontakt zu dem jeweiligen FCM zu erwarten. In Kaltwasserextrakten von FCM aus Papier und Karton gemäß DIN EN 645 wurden Naphthol AS, NAAX, NDPA und HNS im Bereich von 2 bis 368 µgkurz fürMikrogramm/l nachgewiesen. Die daraus resultierende Exposition ist in Tabelle 4 zusammengefasst.
Während die getesteten Trinkhalme keine der organischen Verbindungen enthielten, wurden vor allem in der Produktgruppe des Bäckerrollenpapiers häufig mehrere Analyten in einer Probe quantifiziert. Der höchste Einzelwert wurde im Wasserextrakt eines Blockbodenbeutels bestimmt (HNS, 368 µgkurz fürMikrogramm/l).
Neben diesen vier Verbindungen wurden in einigen Kaltwasserextrakten auch potentielle Spaltprodukte quantifiziert, darunter die primären aromatischen Amine Anilin bzw.
2,4-Dimethylanilin (toxikologische Daten siehe Abschnitt 3.1.2). Auffällig dabei ist ein Anilingehalt von 3 µgkurz fürMikrogramm/l in dem Extrakt eines Bäckerrollenpapieres, in dem gleichzeitig der höchste Naphthol AS-Gehalt aller Proben bestimmt wurde (274 µgkurz fürMikrogramm/l, vgl. Tabelle 4). In Extrakten mit geringeren Naphthol AS-Gehalten (2 bis 95 µgkurz fürMikrogramm/l) wurde kein Anilin nachgewiesen. Dies stützt die Vermutung, dass Naphthol AS einen Anilinvorläufer darstellen könnte. Ein statistischer Zusammenhang lässt sich jedoch bei nur einem Messpunkt nicht ableiten. Eine (zufällige) gleichzeitige Verunreinigung durch beide Stoffe ist ebenfalls denkbar. Neu vorgelegte Untersuchungen in Verdauungssimulanzien zeigten keine nachweisbare Spaltung von Naphthol AS (Bittner et al.kurz füret alii (lat. "und andere") 2022).
Tabelle 4
Tägliche Expositionswerte, abgeleitet aus gemessenen Gehalten organischer Verbindungen und ihrer potentiellen Spaltprodukte in Kaltwasserextrakten von Lebensmittelkontaktmaterialien aus Papier und Karton (tägliche Verzehrmenge 1 kgkurz fürKilogramm Lebensmittel).
| Modell | Gehalt in µg/l Extrakt ≡ Orale Exposition in µg/Person/Tag | |||||
| Analyt | Naphthol AS | NAAX | NDPA | HNS | Anilin | 2,4-DMA |
| Probenanzahl gesamt | 51 | 51 | 51 | 51 | 51 | 51 |
| Probenanzahl > Nachweisgrenze | 10 | 22 | 25 | 19 | 1 | 2 |
| Minimalwert* | 2 | 2 | 2 | 7 | 3 | 3 |
| Maximalwert | 274 | 55 | 22 | 368 | 3 | 3 |
| Mittelwert** | 9 | 9 | 3 | 25 | - | - |
| Median* | 7 | 13 | 6 | 24 | - | - |
- zu wenig Datenpunkte
* der Proben mit Analytgehalten oberhalb der NachweisgrenzeLimit of detectionZum Glossareintrag
** Lower bound Ansatz: Analytgehalte unterhalb der NachweisgrenzeLimit of detectionZum Glossareintrag ≡ 0 µgkurz fürMikrogramm/l
2,4-Dimethylanilin wurde in den Kaltwasserextrakten einer Servietten- und einer Bäckerrollenpapier-Probe mit je 3 µgkurz fürMikrogramm/l nachgewiesen. Potentielle Ausgangsverbindungen hierfür stellen NAAX sowie NDPA dar. Beide Verbindungen wurden in den 2,4-Dimethylanilin-haltigen Extrakten quantifiziert. Da jedoch in über zwanzig weiteren Proben NAAX (bis 76 µgkurz fürMikrogramm/l) und NDPA (bis 22 µgkurz fürMikrogramm/l) mit vergleichbaren oder teils höheren Gehalten gefunden wurden, nicht jedoch das 2,4-Dimethylanilin, ist ein ausschließlicher Zusammenhang zwischen den Gehalten an 2,4-Dimethylanilin und NAAX bzw. NDPA unwahrscheinlich. Neu vorgelegte Untersuchungen in Verdauungssimulanzien zeigten nur eine sehr geringe Spaltung von NAAX bzw. NDPA (Bittner et al.kurz füret alii (lat. "und andere") 2022).
Unter Anwendung der Vorgabe aus der Verordnung (EU) Nr. 10/2011, nach der die tägliche Verzehrmenge eines Erwachsenen 1 kgkurz fürKilogramm Lebensmittel beträgt, ergeben sich die in Tabelle 4 aufgeführten täglichen Expositionswerte.
3.1.4 Risikocharakterisierung
2,4-Dimethylanilin wurde in den Kaltwasserextrakten einer Servietten- und einer Bäckerrollenpapier-Probe mit je 3 µgkurz fürMikrogramm/l nachgewiesen. Potentielle Ausgangsverbindungen hierfür stellen NAAX sowie NDPA dar. Beide Verbindungen wurden in den 2,4-Dimethylanilin-haltigen Extrakten quantifiziert. Da jedoch in über zwanzig weiteren Proben NAAX (bis 76 µgkurz fürMikrogramm/l) und NDPA (bis 22 µgkurz fürMikrogramm/l) mit vergleichbaren oder teils höheren Gehalten gefunden wurden, nicht jedoch das 2,4-Dimethylanilin, ist ein ausschließlicher Zusammenhang zwischen den Gehalten an 2,4-Dimethylanilin und NAAX bzw. NDPA unwahrscheinlich. Neu vorgelegte Untersuchungen in Verdauungssimulanzien zeigten nur eine sehr geringe Spaltung von NAAX bzw. NDPA (Bittner et al.kurz füret alii (lat. "und andere") 2022).
Unter Anwendung der Vorgabe aus der Verordnung (EU) Nr. 10/2011, nach der die tägliche Verzehrmenge eines Erwachsenen 1 kgkurz fürKilogramm Lebensmittel beträgt, ergeben sich die in Tabelle 4 aufgeführten täglichen Expositionswerte.
3.2 Unsicherheitsanalyse
Die toxikologische Datenbasis ist für Naphthol AS, NAAX und NDPA sehr klein. Insbesondere fehlen Daten zur Toxikokinetik und zur (sub)chronischen Toxizität. Aus den vorhandenen in vitro Daten scheint es plausibel oder belegt, dass die genannten Verbindungen im Magen-Darm-Trakt – wenn überhaupt – nur sehr geringe Mengen an Anilinderivaten freisetzen. Unsicherheiten zur Metabolisierung der Stoffe im Körper (z. B. in der Leber) bleiben jedoch.
Für HNS ist die Datenlage etwas umfangreicher. Es konnte eine tolerierbare tägliche Aufnahmemenge abgeleitet werden. Bei ihrer Ableitung sind dennoch vorhandene Unsicherheiten in der Datenlage – wie beispielsweise fehlende Untersuchungen zu Auswirkungen auf die einzelnen Organgewichte oder Blutparameter – einbezogen worden.
3.3 Handlungsrahmen
Für einzelne Proben (n = 2) wurde eine Migration oberhalb von 50 µgkurz fürMikrogramm/kgkurz fürKilogramm Lebensmittel für Naphthol AS beobachtet. Die toxikologische Datenlage ist aktuell nicht ausreichend, um diese Migration gesundheitlich bewerten zu können. Das BfRkurz fürBundesinstitut für Risikobewertung empfiehlt entsprechend, dass kein Übergang von Naphthol AS (sowie von NAAX und NDPA) oberhalb von 50 µgkurz fürMikrogramm/kgkurz fürKilogramm Lebensmittel stattfinden sollte. Materialien mit einer Naphthol AS-, NAAX- oder NDPA-Freisetzung oberhalb von 50 µgkurz fürMikrogramm/l sollten nicht im Kontakt mit Lebensmitteln verwendet werden. Die Freisetzung von HNS sollte 360 µgkurz fürMikrogramm/l nicht übersteigen. Die Hersteller sollten ihre Rohstoffe und Endprodukte auf Verunreinigungen mit diesen Substanzen bzw. deren Freisetzung prüfen und ggf. Alternativen zu den verwendeten Materialien suchen.
4 Referenzen
BAuA (2016) Technische Regeln für Gefahrstoffe. TRGS 905. Verzeichnis krebserzeugender, keimzellmutagener oder reproduktionstoxischer Stoffe. GMBl 2016 S. 378-390 [Nr. 19], Zuletzt geändert und ergänzt: GMBl 2018 S. 259 [Nr.15] In. Externer Link:https://www.baua.de/DE/Angebote/Rechtstexte-und-Technische-Regeln/Regelwerk/TRGS/pdf/TRGS-905.pdf?__blob=publicationFile
Bittner N, Boon A, Delbanco EH, Walter C, Mally A (2022) Assessment of aromatic amides in printed food contact materials: analysis of potential cleavage to primary aromatic amines during simulated passage through the gastrointestinal tract. Arch Toxicol 96(5):1423-1435 doi:Externer Link:10.1007/s00204-022-03254-w
BUA (1992) BUA Stoffbericht 123 - Acetoacetyl-m-xylid. Beratergremium für umweltrelevante Altstoffe der Gesellschaft deutscher Chemiker
ECHAkurz fürEuropäische Chemikalienagentur (2019a) European Chemicals Agency - C&L inventory for 2,6-dimethylaniline (CAS 87-62-7). In. Externer Link:https://echa.europa.eu/information-on-chemicals/cl-inventory-database/-/discli/details/90282
ECHAkurz fürEuropäische Chemikalienagentur (2019b) European Chemicals Agency - Registration dossier for 2'-ethoxy-3-hydroxy-2-naphthanilide (CAS 92-74-0). In. Externer Link:https://echa.europa.eu/registration-dossier/-/registered-dossier/2012/7/7/3
ECHAkurz fürEuropäische Chemikalienagentur (2019c) European Chemicals Agency - Registration dossier for 2'-methoxy-3-hydroxy-2-naphthanilide (CAS 135-62-6). In. Externer Link:https://echa.europa.eu/registration-dossier/-/registered-dossier/22161/7/7/2
ECHAkurz fürEuropäische Chemikalienagentur (2019d) European Chemicals Agency - Registration dossier for 2'-Methoxyacetoacetanilide (CAS 92-15-9). In. Externer Link:https://echa.europa.eu/registration-dossier/-/registered-dossier/14534/7/7/2/?documentUUID=2d2d9d34-3df6-401f-b561-60bde9c933b8
ECHAkurz fürEuropäische Chemikalienagentur (2019e) European Chemicals Agency - Registration dossier for 2'-methyl-3-hydroxy-2-naphthanilide (CAS 135-61-5). In. Externer Link:https://echa.europa.eu/registration-dossier/-/registered-dossier/13267/1
ECHAkurz fürEuropäische Chemikalienagentur (2019f) European Chemicals Agency - Registration dossier for 2'-Methylacetoacetanilide (CAS 93-68-5). In. Externer Link:https://echa.europa.eu/registration-dossier/-/registered-dossier/22153
ECHAkurz fürEuropäische Chemikalienagentur (2019g) European Chemicals Agency - Registration dossier for 2',4'-dimethylacetoacetanilide (CAS 97-36-9). In. Externer Link:https://echa.europa.eu/registration-dossier/-/registered-dossier/14428
ECHAkurz fürEuropäische Chemikalienagentur (2019h) European Chemicals Agency - Registration dossier for 2,4-dimethylaniline (CAS 95-68-1). In. Externer Link:https://echa.europa.eu/de/registration-dossier/-/registered-dossier/2085/7/7/2
ECHAkurz fürEuropäische Chemikalienagentur (2019i) European Chemicals Agency - Registration dossier for 3-hydroxy-2-naphthoic acid (CAS 92-70-6). In. Externer Link:https://echa.europa.eu/registration-dossier/-/registered-dossier/14175
ECHAkurz fürEuropäische Chemikalienagentur (2019j) European Chemicals Agency - Registration dossier for 4'-methoxy-3-hydroxy-2-naphthanilide (CAS 92-79-5). In. Externer Link:https://echa.europa.eu/registration-dossier/-/registered-dossier/22153
ECHAkurz fürEuropäische Chemikalienagentur (2019k) European Chemicals Agency - Registration dossier for 6-Hydroxy-2-naphthoic acid (CAS 16712-64-4). In. Externer Link:https://echa.europa.eu/registration-dossier/-/registered-dossier/10731/7/7/3
ECHAkurz fürEuropäische Chemikalienagentur (2019l) European Chemicals Agency - Registration dossier for Acetoacetanilide (CAS 102-01-2). In. Externer Link:https://echa.europa.eu/registration-dossier/-/registered-dossier/22153
ECHAkurz fürEuropäische Chemikalienagentur (2019m) European Chemicals Agency - Registration dossier for aniline (CAS 62-53-3). In. Externer Link:https://echa.europa.eu/de/registration-dossier/-/registered-dossier/15333/7/8
EDI (2017) Verordnung des Eidgenössischen Departement des Innern (EDI) über Materialien und Gegenstände, die dazu bestimmt sind, mit Lebensmitteln in Berührung zu kommen (Bedarfsgegenständeverordnung) - Anhang 10 (Druckfarben). In. Externer Link:https://www.blv.admin.ch/dam/blv/de/dokumente/lebensmittel-und-ernaehrung/rechts-und-vollzugsgrundlagen/lebensmittelrecht2017/anhang10-verordnung-materialien-kontakt-lm-gg.pdf.download.pdf/Anhang_10.pdf
EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit) Panel on Food Additives F, Processing Aids, Food Micw, Aguilar F, et al.kurz füret alii (lat. "und andere") (2008) Note for Guidance For the Preparation of an Application for the Safety Assessment of a Substance to be used in Plastic Food Contact Materials. EFSAkurz fürEuropean Food Safety Authority (Europäische Behörde für Lebensmittelsicherheit) Journal 6(7):21r doi:Externer Link:10.2903/j.efsa.2008.21r
EU (2004) European Union Risk Assessment Report. 1st Priority List. Volume 50. Aniline. Institute for Health and Consumer Protection of the European Chemicals Bureau
Fukami T, Kariya M, Kurokawa T, Iida A, Nakajima M (2015) Comparison of substrate specificity among human arylacetamide deacetylase and carboxylesterases. European Journal of Pharmaceutical Sciences 78:47-53
doi: Externer Link:10.1016/j.ejps.2015.07.006
GDCh Beratergremium für umweltrelevante Altstoffe (BUA). In. Externer Link:https://www.gdch.de/fileadmin/downloads/Publikationen/Weitere_Publikationen/PDF/bua_infoallgemein.pdf
JCHECK (2019) Japan Chemicals Collaborative Knowledge Database - entry for 3-Hydroxy-2-naphthanilide ( 92-77-3 ).
JECDB Japan Existing Chemical Database - Test report - Exp. No. 7817 (115-182): in vivo Micronucleus test for 3-Hydroxy-2-naphthoic acid ( 92-70-6 ).
JECDB (2000) Japan Existing Chemical Database - Test report - One-geration Reproductive Toxicity Test for 3-Hydroxy-2-naphthoic acid ( 92-70-6 ).
JECDB (2019a) Japan Existing Chemical Database - entry for 3-Hydroxy-2-naphthanilide ( 92-77-3 ).
JECDB (2019b) Japan Existing Chemical Database - entry for o-Acetoacetotoluidide ( 93-68-5 ).
Kobayashi Y, Fukami T, Higuchi R, Nakajima M, Yokoi T (2012) Metabolic activation by human arylacetamide deacetylase, CYP2E1, and CYP1A2 causes phenacetin-induced methemoglobinemia. Biochemical Pharmacology 84(9):1196-1206 doi:Externer Link:10.1016/j.bcp.2012.08.015
Lipinski CA, Lombardo F, Dominy BW, Feeney PJ (2001) Experimental and computational approaches to estimate solubility and permeability in drug discovery and development settings1PII of original article: S0169-409X(96)00423-1. The article was originally published in Advanced Drug Delivery Reviews 23 (1997) 3–25.1. Advanced Drug Delivery Reviews 46(1):3-26, doi: Externer Link:10.1016/S0169-409X(00)00129-0
OECD (2004) SIDS Initial Assessment Report For SIAM 19 - 3-Hydroxy-2-naphthoic acid.
Rasper TO (2016) Primäre aromatische Amine und Präkursoren in Pigmenten, Druckfarben und bedruckten Papieren. Diplomarbeit, Technische Universität Dresden
Sabbioni ABG (1999) Biomonitoring of arylamines: haemoglobin adducts of aniline derivatives. Biomarkers 4(3):229-236 doi: Externer Link:http://dx.doi.org/10.1080/135475099230895
Shimizu M, Fukami T, Ito Y, et al.kurz füret alii (lat. "und andere") (2014) Indiplon is Hydrolyzed by Arylacetamide Deacetylase in Human Liver. Drug Metabolism and Disposition doi:Externer Link:10.1124/dmd.113.056184
Toxnet CCRIS/Toxnet Datenbank-Eintrag für N-Acetoacetyl-p-toluidin (2415-85-2).
Watanabe A, Fukami T, Nakajima M, Takamiya M, Aoki Y, Yokoi T (2009) Human Arylacetamide Deacetylase Is a Principal Enzyme in Flutamide Hydrolysis. Drug Metabolism and Disposition 37(7):1513-1520 doi: Externer Link:http://dx.doi.org/10.1124/dmd.109.026567
Yoshida T, Fukami T, Kurokawa T, Gotoh S, Oda A, Nakajima M (2018) Difference in substrate specificity of carboxylesterase and arylacetamide deacetylase between dogs and humans. European Journal of Pharmaceutical Sciences 111:167-176 doi: Externer Link:10.1016/j.ejps.2017.09.040
Zeiger E, Anderson B, Haworth S, Lawlor T, Mortelmans K (1992) Salmonella mutagenicity tests: V. Results from the testing of 311 chemicals. Environmental and Molecular Mutagenesis 19(S21):2-141 doi: Externer Link:10.1002/em.2850190603
Weitere Informationen auf der BfRkurz fürBundesinstitut für Risikobewertung-Website zu Lebensmittelkontaktmaterialien
- Fragen und Antworten: Näher erklärt: BfRkurz fürBundesinstitut für Risikobewertung-Empfehlungen zu Materialien für den Lebensmittelkontakt Zur FAQ
- Gesundheitliche Bewertung von Materialien in Kontakt mit Lebensmitteln Zur Seite
- BfRkurz fürBundesinstitut für Risikobewertung-Empfehlungen zu Materialien für den Lebensmittelkontakt Zur Seite